Con el objetivo de informar a las empresas asturianas sobre las condiciones y requerimientos legales para la exportación de dispositivos médicos a Estados Unidos, Asturex organizó, el pasado 12 de junio, un webinar en colaboración con Kaeltia Consulting, focalizado en los requerimientos que deben cumplir este tipo de productos ante la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA).
Para la FDA, un dispositivo médico es un instrumento, aparato, máquina, implante, reactivos de diagnóstico, software o cualquier otro artículo utilizado para el diagnóstico, tratamiento o prevención de enfermedades en seres humanos, o para modificar la estructura o función del cuerpo. Esto incluye desde simples suministros médicos hasta complejos sistemas de diagnóstico y equipos quirúrgicos. De ahí la importancia de conocer toda la normativa que la entidad reguladora exige a los equipos importados a este mercado.
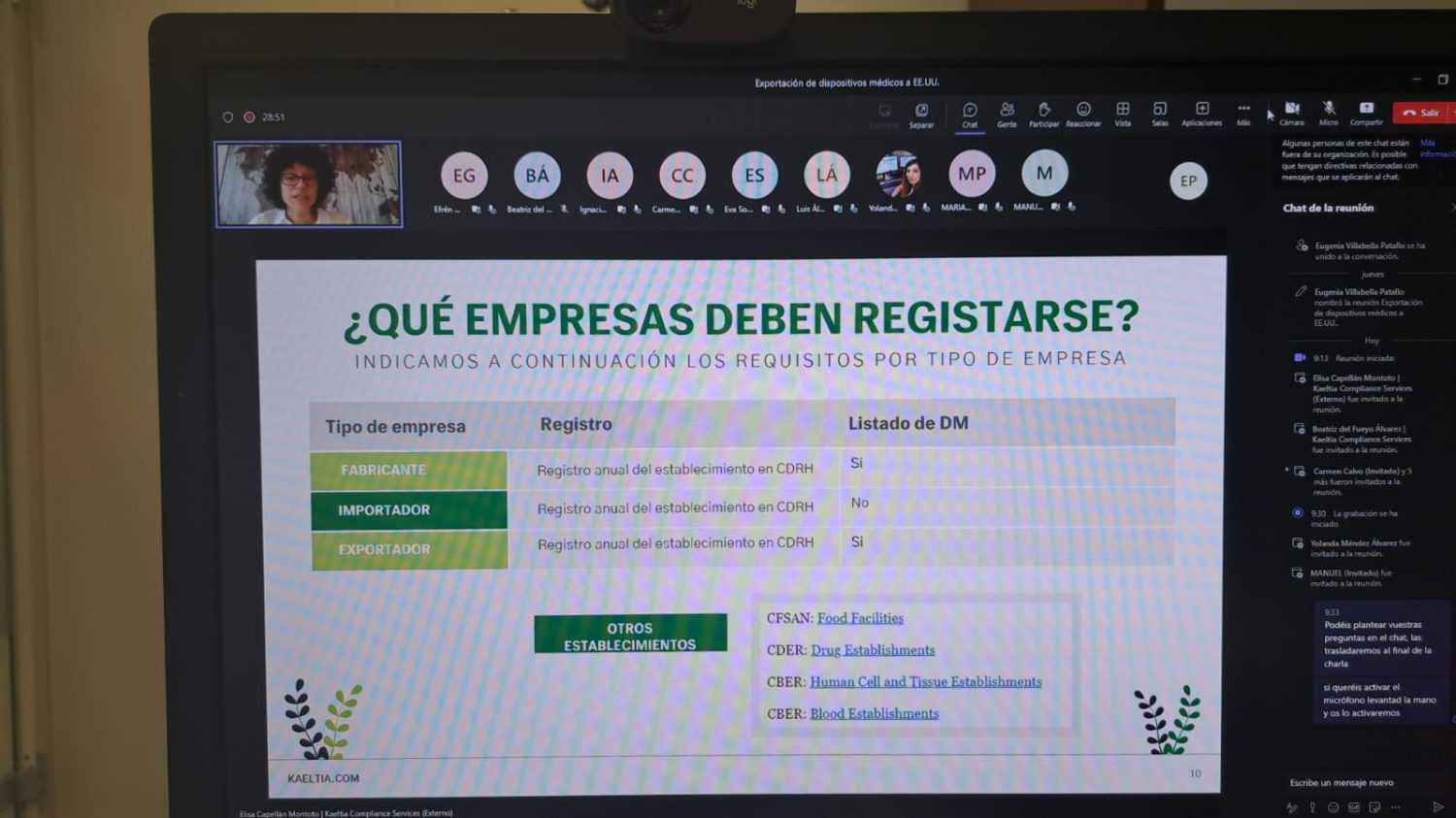
Las 13 empresas participantes destacaron la importancia de esta jornada en la que la Dra. Elisa Capellán Montoto, CEO y consultor senior de Asuntos Reglamentarios, repasó las diferentes categorías de dispositivos médicos, las normas de etiquetado y los requisitos de importación, entre otros temas destacados. El webinar también ofreció información sobre todos los trámites del producto ante la FDA y el registro y listado de exportadores, además de dar respuesta a las preguntas individuales de cada participante.
Accede a la grabación del webinario aquí: ACCESO A GRABACIÓN WEBINARIO
Aparecido en medios
- Asturex informa a empresas sobre los requerimientos legales para la exportación de dispositivos médicos a Estados Unidos – Empresa Exterior